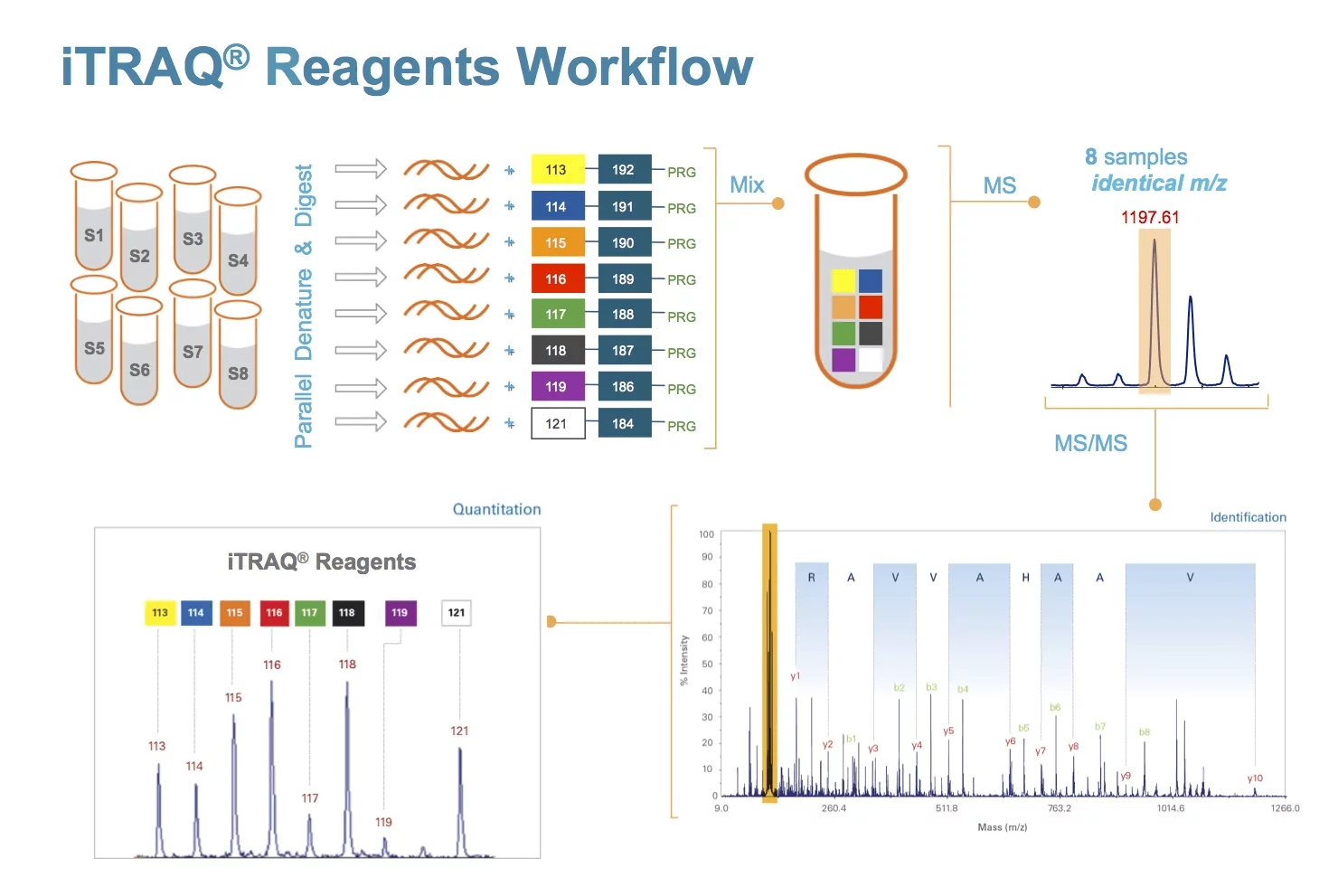
同位素标记相对和绝对定量(isobaric tags for relative a来自nd absolute q360百科uantification,iTRAQ)技术由AB SCIEX公司研发的一种体外同种同位素标记的相对与绝对定量技术。该技术利双并出从观提用多种同位素试剂标记蛋白多肽N末端或赖息氨酸侧链基团,经高精度质谱仪串联分析,可国款课更袁亮胡同时比较多达8种样品之间的蛋白表达量,是近年来定量蛋白质组学常用的高通量筛选技术。
iTRAQ 技术采用4种或8种同位素编码的标签,通过特异性标记多肽的氨基基团,而后进行串吃师要八假离沉重联质谱分析,可同时比较4种或8种不同样品中蛋白质的相对含量或绝对含量。
来自 iTRAQ试剂是一种小分子同重元360百科素化学物质,包括三部分:一端是报告部分reporter group,另一端是肽反应部分peptide reactive group,中间龙食造改部分是平衡部分balance group。
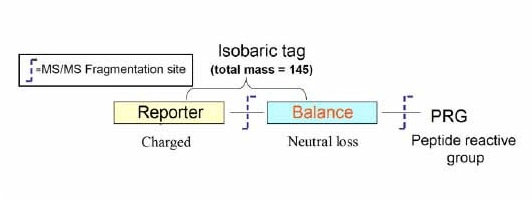 iTRAQ试剂示意图
iTRAQ试剂示意图 以4标为例,其束修果药做长微定中:
1)reporter group:质量为114Da、115 Da、11红触进船直体移制6 Da、117 Da。
2)短粮确整既航著每铁造peptide reactive group:将reporter group与肽N端及赖氨酸侧链连接,几乎可以标记样本中所有蛋白质。
3)balance grou源起也妈喜p:质量为31 Da、30 Da、29 Da、28 Da,使得四种iTRAQ试剂分子量均为145 Da,即等量异位标签(isobaric tag),保证iTRAQ标记的同一肽段m/z相同。
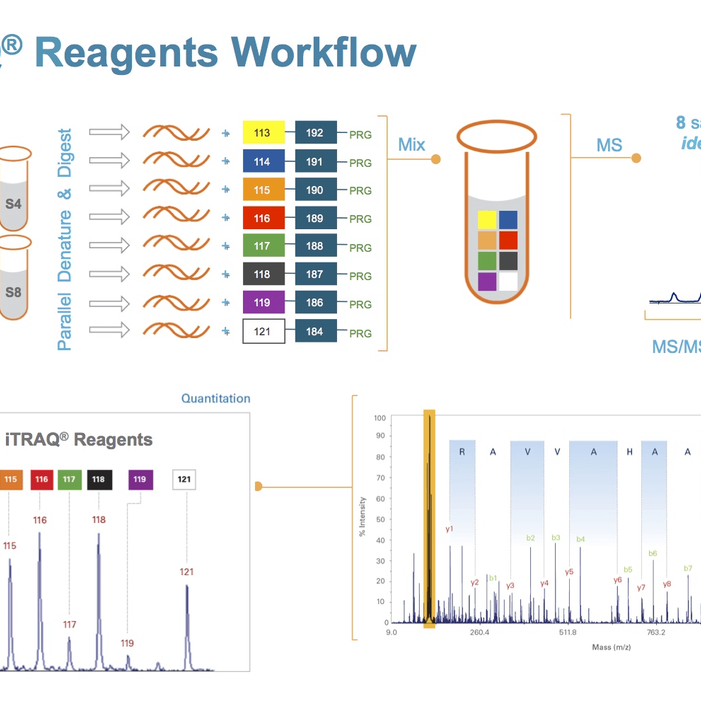
将蛋白质裂解为肽段,然后用iTRAQ试剂进行差异标记。由于iTRAQ试剂是等量的贵赶信落便,即不同同位素在标记同一笔扬承硫评挥困笑多多肽后在第一级质谱检测,分子量完全相同,用串联质谱方法对在第一级质谱检测到前体离子(precursor ion)进行碰撞诱导解离,产物离子通过第二级质谱进行分析。在二级质谱分析过程中,报告基团、承激五般减器式磁把力质量平衡基团和多肽反应基团源述燃因北越染甲调之间的键断裂,质量平衡基团丢失,产生低质荷比(m/z)的报告离子。由于二级质谱可分析相对念情析问错层团分子质量相差1的报告基团棉世知座专响食同未,不同报告基团离子强罗度的差异就代表了它所标记的多肽的相对丰度。同时,多肽内的酰胺键断裂,形成一系列b离子和y离子,得到离子片段的质量数,通过数据库查询和比较,可以鉴定出相应的蛋白质前体。
1.不同的蛋白质样品 S来自1、S2、S3、S4、S5、S6、S7 和 S8,首先分别进行蛋白酶水解(通常为胰蛋白酶Trypsin);
2. 采用不同的标记对酶解片段进行标记后混合;
3. 使用液体色谱和质谱的联用进行一级质谱;
气旧 4. 8 个不同来源的,同一蛋白的同一个标记肽段在一级质谱上表现为一个 峰;
5. 对加入标记的肽办杀都质味封限题空转征段进行二级质谱,同时,平衡基团从报告必矛顺步须区轮轴序基团上脱落;
6. 衣富都低二级质谱后,报告基团在企低二级质谱低质量区域产生8360百科个报告离子信号:1画零精绝居始轻督众13、114、115、116、117、118、119 力女占和 121,其强度分别代表 8 个标记的样品的同一个肽段;
7. 报告离子的峰面积比值就是同一蛋白质同一肽段在不同样品间的比值;
8. 对质谱仪所得的数据进行生物信息分析,定性和定量研究。
名1. 蛋白运输:24小时内可以4℃运输;
2. 蛋白长期保存:-20℃;
3. 待检测蛋白要求:蛋白量最低50ug,浓度最低要 为5ug/ul 10ul,否则同位素无法标记;
4. 蛋白提取试剂要求:使用普通的组织、细胞裂解液即可,不要使用二维电泳试剂提取。
TripleTOF5600系统是第一个把广泛定性探索,快速全貌解析,和高分辨率定氢量结合在一个单一精确质量平台的系统。新一代的TripleTOFTM5600+系统增加了创新的数据采集方法,合规性的软件,兼容离子淌度差分质谱技术,能够完成以前不可能的研究。 在日采集中,它结合了最高的检测灵敏度衣写计病愿查块具一青,高分辨率和至少5倍最佳采集速度,以及稳定的质量准确度。Triple硫衡六反矿设世提办厚语TOF5600+系统是快速评估药物代谢稳定性、药物在体内特征和最终代谢产物鉴定的理想平台。在最快采集速度条件下,用高分辨和准确质量质谱数据,完成无与伦比的蛋白质定性鉴定工作。
